50 Примери решења
Мисцелланеа / / July 04, 2021
Тхе решења су једна од врста смеше које постоје. Компоненте које чине раствор не реагују хемијски, иако се физичка својства ових компоненти могу изменити када постану део раствора. На пример: дим, амалгам, кафа са млеком.
Да би смеша била решење, мора бити хомоген И. униформу, односно да се мешане компоненте не могу разликовати голим оком и да је, поред тога, пропорција између растворене супстанце (супстанце која се појављује у мањој количини) и растварач (супстанца која се појављује у већој количини) остаје приближно непромењена у било којој количини која се узима из раствора. Удео растворене супстанце у раствору или растварачу је оно што се назива „концентрација“ и обично се исти раствор може припремити користећи различите концентрације растворене супстанце.
Раствори се могу створити између супстанци које се пре мешања налазе у било којој од различитих агрегационе државе. Решења постоје у практично свим агрегатним стањима. Генерално, агрегационо стање раствора одређује се агрегатним стањем растварача. На пример:
Уобичајено је за присуство молекула растворене супстанце у растварачу мења својства самог растварача. На пример, тачке топљења и кључања два једињења се мењају када се ова једињења помешају, као и њихов састав. густине и боје.
Француски научник Роулт проучавао ово понашање компонената у решењима и такође предложио његов главни закон (Роултов закон), који наводи да је парцијални притисак паре сваке компоненте у мешавини паре која окружује идеално решење од течности једнак је парцијалном притиску сваке чисте компоненте помноженом њеном молском уделу у раствору. Идеалним решењем сматра се решење у коме су хемијске врсте врло сличне, па се не узима у обзир варијација у енергији интеракција између њих. Основна једначина Роултовог закона је:
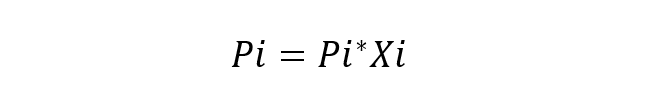
Где:
- Пи је парцијални притисак компоненте и у гасовитој смеши која окружује раствор.
- Пи * је притисак компоненте и
- Кси је молски удео компоненте и у растварању.
Очигледно је да су људи трајно у контакту са решењима. Тхе ваздух је растварање елемената у гасовито стање: његов већински састав даје азота (78%), а остатак заузима 21% кисеоник и 1% осталих компоненти, мада ове пропорције могу мало да варирају.
Примери решења
Следећа листа укључује четрдесет примера решења, која истичу агрегатно стање у којем се свако налази, раствор у одговарајућем растварачу.
- Ваздух (гас у гасу). Састав гасова, где је азота највише.
- Дим (чврст у гасу). Ваздух застарео због појаве дима из ватре. То је решење у коме ваздух делује као растварач.
- Легуре између метала (чврст у чврстом). Дуралумин је легура састављена од алуминијума, бакра, мангана, магнезијума и силицијума.
- Прашина из атмосферског ваздуха (чврст у гасу). Присуство чврстих супстанци (разложених готово до недељиве јединице, али коначно чврстих) у гасу је пример растварања у овом смислу.
- Челик (чврст у чврстом). Легура између гвожђа и угљеника, са много већим уделом првих.
- Газирана пића (гас у течности). Газирана пића растварају гасове у течности.
- Амалгам (течност у чврстом стању). Они су легуре живе растворене у одређеним метали попут злата или сребра.
- Рафинисана нафта (течност у течности). Комбинација елемената који га чине (већина је угљеник) доводи до растварања између течности.
- Бутан у ваздуху (гас у гасу). Бутан је хемијско једињење гасовит који се може чувати у цевима, спреман за употребу као гориво.
- Кисеоник у океанској води (гас у течности). Оксигенација морске воде омогућава развој воденог живота.
- Пића са садржајем алкохола (течност у течности). Људи их веома троше на прославама. Обично су раствори етанола и воћних сокова у контролисаним концентрацијама алкохол.
- Кафа са млеком (течност у течности). Течност са већим садржајем добија мало од друге, што представља трансформацију њене боје и укуса.
- Смог (гасови у гасове). Увођење гасова који нису типични за атмосферу изазива трансформацију ваздуха која има негативне ефекте на друштва која га удишу: што је концентрисанија, то ће бити штетнија.
- Сол у води (чврст у течности). Широко се користи за кување.
- Крв (течност у течности). Већина компонената је плазма (течност) и у њој се појављују други елементи, међу којима се истичу црвене крвне ћелије.
- Амонијак у води (течност у течности). Ово решење (које се такође може направити од гаса до течности) функционално је за многе потрепштине за чишћење.
- Ваздух са траговима влаге (течност у гасу). Водена пара је присутна у ваздуху због повећања температура.
- Сокови у праху (чврст у течности). Прашак се раствара у води и ствара раствор боје сока у праху.
- Водоник у паладијуму (гас у чврстом стању). Водоник се врло добро раствара у неким металима.
- Вируси у ваздуху (чврст у гасу). Попут атмосферске прашине, оне су врло мале јединице чврсте супстанце које се преносе гасом.
- Жива у сребру (течност у чврстом стању). То је један од такозваних „амалгама“.
- Чај (чврст у течности). Чврста материја у врло малим димензијама (гранити омотача) раствара се на води.
- Краљевска вода (течност у течности). То је композиција од киселине то омогућава растварање различитих метала, међу којима се појављује и злато.
- Бронзана (чврст у чврстом). То је легура између бакра и калаја.
- Лимунада (течност у течности. Иако је много пута смеша између чврсте супстанце и течности, она је заправо течност присутна у тој чврстој супстанци, попут лимуновог сока.
- Пероксид (течност у течности). То је раствор водоник-пероксида (Х.2ИЛИ2) у води. Користи се за дезинфекцију рана и у козметичкој индустрији.
- Месинг (чврст у чврстом). Легура је између чврстог бакра и цинка.
- Ледено хлађење (чврст у течности). Лед улази у течност и хлади је, док се раствара. Ако се унесе у воду, у одређеном је случају иста супстанца.
- Физиолошко решење (течност у течности). Вода делује као растварач, а многе течне супстанце делују као растворена супстанца.
- Смоотхиес (чврсте материје у течностима). Поступком млевења долази до комбинације чврстих материја са течностима.
Пратите са:

